近日,基础医学院医学遗传学教研室徐湘民和生物化学与分子生物学教研室潘星华领衔的研究团队在《PNAS》杂志上发表了题为“Putative Regulators for the Continuum of Erythroid Differentiation Revealed by Single-Cell Transcriptome of Human BM and UCB cells”的研究论文。2019届毕业博士生黄朋、美国Cleveland Clinic赵永忠和2020届毕业硕士生钟健美为该论文并列第一作者,徐湘民和潘星华为共同通讯作者。
《PNAS》全称Proceedings of the National Academy of Sciences of the United States of America,是美国科学院院报,于1914年创立,是世界上被引最多的综合性、跨学科连续出版物之一,2019年影响因子为9.58。
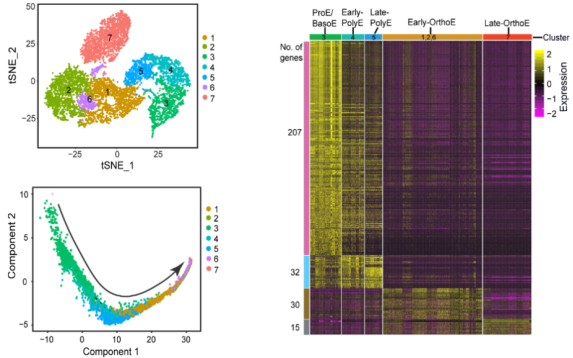
该研究首次报道在单个细胞水平上,对处于不同分化时期的原始红细胞的基因表达水平进行研究,揭示了调节红细胞分化、成熟的基因调控网络。因受到人体内所含有的原始红细胞(终末期分化红细胞)数量少和没有特异性细胞表面抗原来分选各分化时期的红细胞限制,传统的RNA测序方法无法直接对它们进行研究。近十几年来,研究人员试图用小鼠细胞或者体外培养的人类细胞来解析相关问题,虽然取得了一些重大的发现,但是人体内原始红细胞的精准研究仍然缺乏,对它们的研究遇到了瓶颈。徐湘民教授的研究采用单细胞转录组测序技术(10x Genomics)对成人骨髓和新生儿脐带血来源的原始红细胞的基因表达水平进行精准研究和分析,突破了研究“瓶颈”,成功对各个分化时期的红细胞基因表达水平进行分析,揭开了终末期红细胞造血的“真面目”。该研究成果主要包括以下几点:将中幼红细胞和晚幼红细胞进行了细分,有助于贫血亚型的分类和识别;揭示了终末期红细胞基因表达的变化轨迹;发现了一系列在不同的分化时期起调节作用的转录因子。该研究成果将促进红细胞造血的研究进入一个新的时期,为研究红细胞终末期造血以及红细胞脱核机制等提供新的思路,以及为研究红细胞造血相关疾病的发病机制提供理论依据。
论文链接为:https://www.pnas.org/content/117/23/12868










